Sin embargo, los anticuerpos, las moléculas diseñadas a medida por nuestro sistema inmune se pueden fabricar en serie. ¿Lograrán ser la reina del tablero y poner en jaque a la corona vírica?
Comienza la partida
Las primeras fichas se basaron en el reposicionamiento de fármacos, una de las estrategias más rápidas y seguras de identificar fármacos.
Se crearon diferentes plataformas, como Solidaridad o REMAP-CAP para probar la eficacia de estos medicamentos ya conocidos (tabla 1). Se utilizaron métodos innovadores, probando simultáneamente múltiples combinaciones de potenciales terapias, a diferencia de los ensayos tradicionales, en los que se estudia solo un fármaco en un proceso mucho más lento.
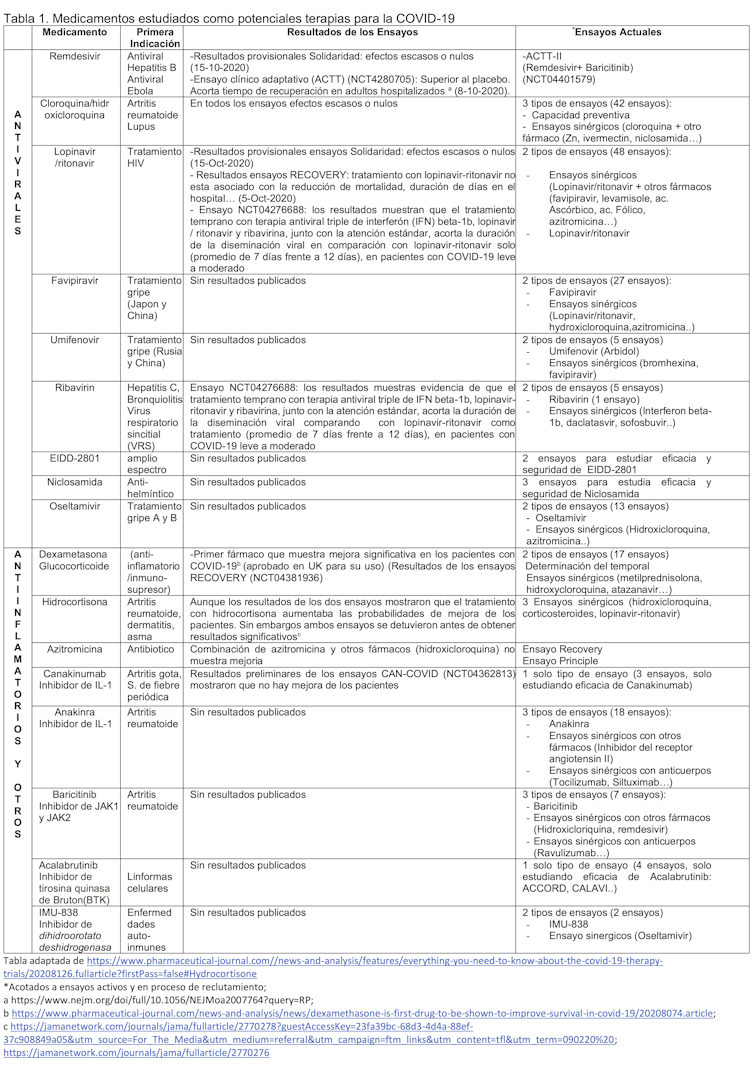
Nuria Campillo, Author provided
Recientemente han sido confirmados los resultados negativos del ensayo Solidaridad. Los ensayos de los cuatro tratamientos evaluados (remdesivir, hidroxicloroquina, lopinavir/ritonavir e interferón) han mostrado efectos escasos o nulos, tanto al nivel de mortalidad general, como en el tiempo transcurrido hasta la iniciación de la respiración mecánica o la duración de la hospitalización en pacientes ingresados.
Además de antivirales y antiinflamatorios, se han estudiado otros compuestos, como la vitamina C y la colchicina. Desafortunadamente, como observamos en la tabla, los resultados de los ensayos no han sido muy alentadores.
Tampoco el tratamiento con plasma de supervivientes, que surgió como primera terapia rápida y asequible, es válido. Los riesgos que conlleva han desestimado su utilización.
Anticuerpos monoclonales, ¿la terapia definitiva?
Pero aún tenemos fichas en el tablero para contraatacar. De los 319 ensayos de compuestos actualmente contra la covid-19, 80 estudios corresponden a anticuerpos como agentes terapéuticos. Cerca de una decena se encuentran ya en fase III, y otros tantos en fase II. Esto significa que están muy cerca de su aprobación definitiva.
Los anticuerpos (también conocidos como inmunoglobulinas), son proteínas en forma de Y (figura 1) que flotan en la sangre y son capaces de pegarse (unirse con mucha afinidad) a una proteína de una bacteria o virus (llamada antígeno). El patógeno queda así desactivado o marcado para que el resto del sistema inmune lo pueda detectar y destruir.
Los anticuerpos son segregados por las llamadas células B plasmáticas, que aparecen en la sangre cuando comienza una infección. Cada anticuerpo es específico para un antígeno. Gran parte de se estructura es común para todos ellos, pero hay unas pequeñas zonas en los extremos superiores de la Y, llamadas regiones variables, que son distintas y reconocen específicamente a diversos patógenos.
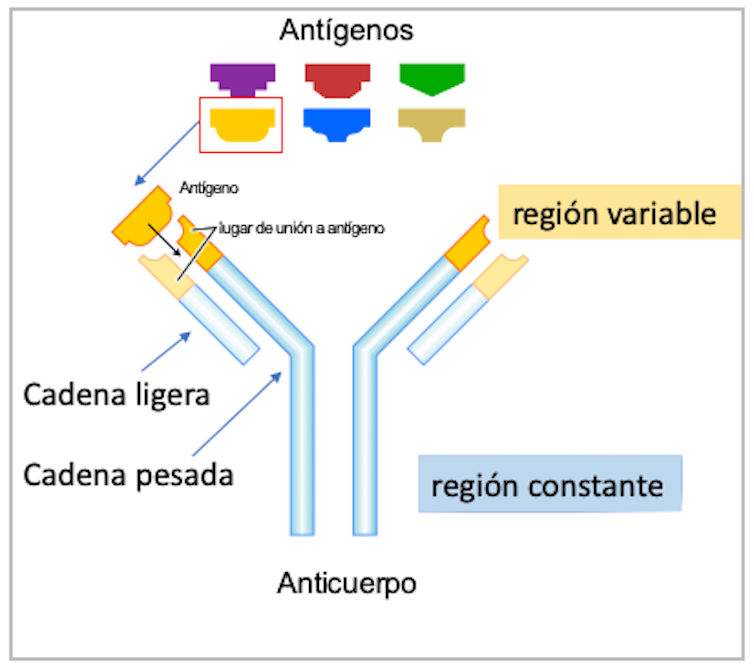
Gustavocarra, adaptado por Mercedes Jiménez, Author provided
Esta gran diversidad de células productoras de anticuerpos aparece en el ser humano durante el desarrollo infantil, como consecuencia de combinaciones al azar y posteriores mutaciones en los genes que codifican esas regiones variables. De esta manera, cuando el ser humano alcanza la adolescencia, ya tiene en su organismo un bagaje de células B capaces de producir anticuerpos contra una infinidad de posibles infecciones.
¿Cómo se producen fuera de nuestro cuerpo?
El diseño de los anticuerpos para actuar contra dianas concretas en enfermedades e infecciones comenzó a partir de 1975 con el trabajo de Khöler y Milstein. Estos investigadores fusionaron células de ratón y células de crecimiento ilimitado (procedentes de tumores) poniendo a punto los hibridomas, resultado por el que recibieron el premio Nobel en 1984.
Los anticuerpos monoclonales, altamente específicos y producidos de forma ilimitada, son purificados y utilizados terapéuticamente (figura 2).
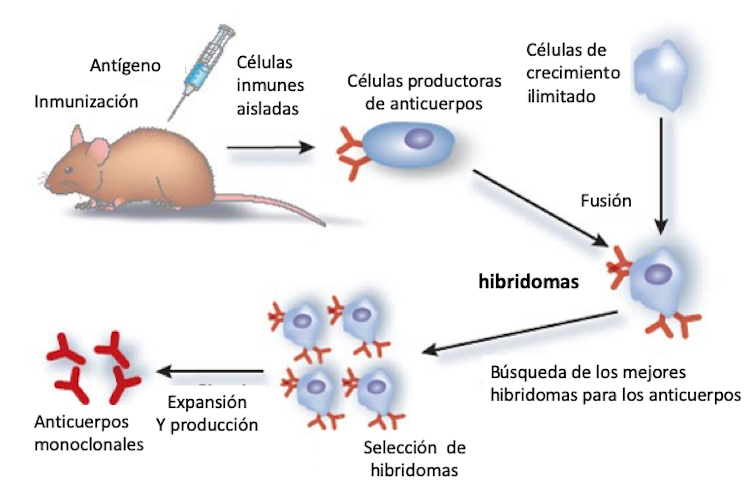
El primer anticuerpo monoclonal terapéutico, el muromonab, se desarrolló para el rechazo en trasplantes y fue aprobado en 1986. Pero debido a su origen no humano, presentaba efectos adversos.
Gracias a las técnicas de ingeniería genética, los anticuerpos monoclonales han sido progresivamente modificados de manera que se parezcan cada vez más a los anticuerpos humanos, evitando problemas de tipo inmunológico (figura 3).
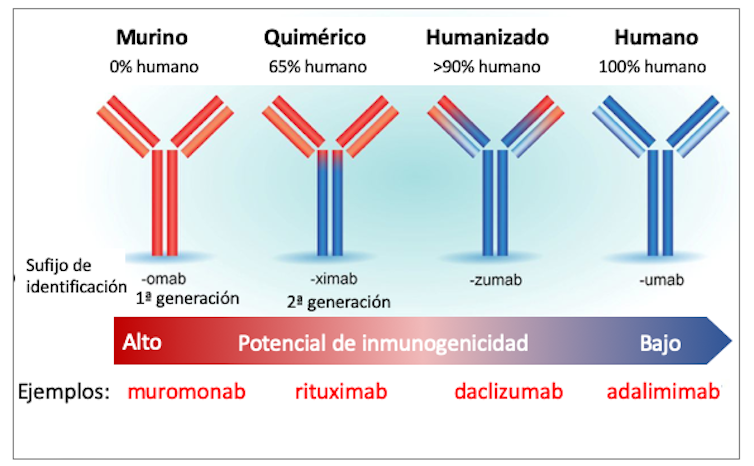
Adaptado de Foltz (2013) por Mercedes Jiménez, Author provided
Actualmente, comenzando a pequeña escala a partir de la elaboración en cultivos de laboratorio se producen a gran escala y se transforman para su posterior formulación y administración (figura 4).
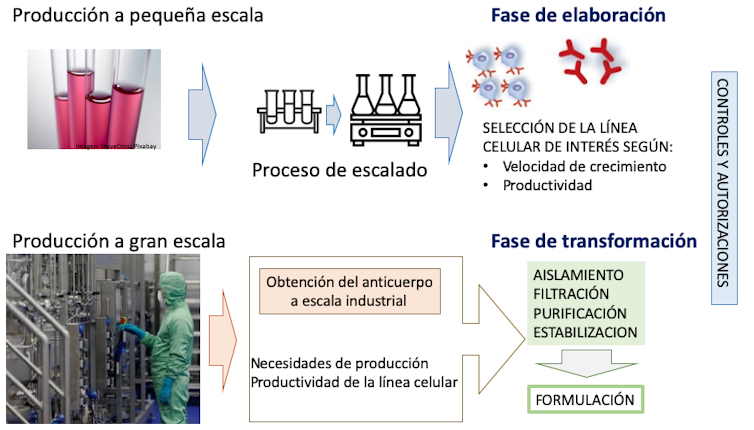
Adaptado de Villaescusa (2017) por Mercedes Jiménez, Author provided
El primer anticuerpo monoclonal aprobado para su uso contra la covid-19 ha sido el bamlanivimab, autorizado en EE. UU. de forma condicional puesto que los datos de seguridad y eficacia no han sido aún contrastados por la comunidad científica. Las autoridades reguladoras decidieron aprobarlo anticipadamente debido a la situación de emergencia, con el compromiso de que esos datos se tienen que hacer públicos en un breve tiempo.
Por último, hay que destacar que la capacidad de los anticuerpos no es solo terapéutica. También pueden utilizarse como profilaxis mediante una vacunación pasiva. Recientemente se ha demostrado que, aunque la inmunidad aportada no fuera duradera, conseguiría proteger del contagio. Esta doble acción podría otorgar a los anticuerpos, además de una esperanza, el papel de dama en el tablero.
Todavía no conocemos el resultado de la partida, pero en las actuales circunstancias, un tratamiento, si es efectivo, significa mucho. El jaque mate definitivo está más cerca.![]()
María Mercedes Jiménez Sarmiento, Científica del CSIC. Bioquímica de Sistemas de la división bacteriana. Comunicadora científica, Centro de Investigaciones Biológicas Margarita Salas (CIB – CSIC); Matilde Cañelles López, Investigadora Científica. Ciencia, Tecnología y Sociedad y Nuria Eugenia Campillo, Científico Titular. Medicinal Chemistry, Centro de Investigaciones Biológicas Margarita Salas (CIB – CSIC)
Este artículo fue publicado originalmente en The Conversation. Lea el original.

